納米等離子體超表面技術(shù)以其高靈敏度而聞名,在癌癥檢測領(lǐng)域備受關(guān)注。然而,傳統(tǒng)生物傳感方法的數(shù)據(jù)處理和分析效率低下,阻礙了其潛力的發(fā)揮。
2025年9月23日,中國人民解放軍總醫(yī)院第五醫(yī)學(xué)中心Li Bo、李伯安和廈門大學(xué)朱錦鋒共同通訊在Advanced Science在線發(fā)表題為“Deep Learning-Powered Nanoplasmonic Biosensing Approach Enables Ultrasensitive Extracellular Vesicles Profiling for Cancer Screening”的研究論文。該研究提出了一種基于柯爾莫戈洛夫-阿諾德網(wǎng)絡(luò) (KAN) 超表面芯片 (metaEVchip) 的生物傳感策略,用于血清中超靈敏的小細(xì)胞外囊泡 (sEV) 分析。
通過基于 KAN 的深度學(xué)習(xí)納米等離子體生物傳感技術(shù)分析來自 600 例胰腺導(dǎo)管腺癌 (PDAC) 患者和 1200 例對照者的全光譜數(shù)據(jù),該策略在外部驗證集中實現(xiàn)了 0.99 的曲線下面積 (AUC),優(yōu)于傳統(tǒng)方法。進(jìn)一步探索這種增強的性能,揭示了 KAN 同時捕獲多維光譜特征的機制,這一優(yōu)勢能夠?qū)崿F(xiàn)高效的數(shù)據(jù)處理和準(zhǔn)確性。這一進(jìn)步大大擴展了納米等離子體超表面在生物傳感中的適用性,并為癌癥篩查和改善多種惡性腫瘤的臨床管理建立了新的范例。
胰腺導(dǎo)管腺癌 (PDAC) 是最致命的癌癥之一,通常表現(xiàn)為晚期且無法切除,5 年生存率僅為 12%。早期發(fā)現(xiàn)可將生存率提高 30% 至 40%。目前,檢測血清中的糖類抗原 19-9 (CA 19-9) 水平是 PDAC 最廣泛使用的液體活檢方法,但其敏感性和特異性不足,可能導(dǎo)致誤診或漏診。這些局限性凸顯了對更可靠診斷標(biāo)志物的需求。檢測血清中的小細(xì)胞外囊泡 (sEV) 是一種很有前景的替代方法,可提供卓越的非侵入性診斷方法。sEV 是由多種哺乳動物細(xì)胞主動分泌的納米級膜囊泡,尤其是快速分裂的癌細(xì)胞。這些囊泡在血液中含量豐富,在介導(dǎo)細(xì)胞間通訊方面至關(guān)重要。與健康對照 (HC) 相比,腫瘤來源的 sEV 表面富含特異性蛋白質(zhì)。例如,GPC1 和 EphA2 陽性 sEV 在區(qū)分胰腺導(dǎo)管腺癌 (PDAC) 與健康對照及其他疾病患者方面表現(xiàn)出較高的特異性和靈敏度。這些腫瘤特異性標(biāo)記物有望克服 CA 19-9 的局限性,為 PDAC 提供更靈敏、更特異的診斷工具。
在此背景下,納米等離子體超表面利用共振波長下的強局域電場增強,已成為一種強大的工具,可用于無標(biāo)記、無損地識別各種生物樣品。具體而言,分析物的固有特性會引起介電環(huán)境的變化,這表現(xiàn)為超表面響應(yīng)中的波長偏移和強度變化。這些變化與分析物的濃度高度相關(guān),從而為實現(xiàn)精確、靈敏的檢測提供了可能。此外,折射效應(yīng) (RE)、光譜效應(yīng) (SE) 和納米等離子體負(fù)載效應(yīng) (NLE) 分別從不同角度分析光譜響應(yīng),以闡明確定分析物濃度和類型的基礎(chǔ)。然而,僅僅依賴單一的傳感視角可能會導(dǎo)致寶貴信息的丟失,尤其是對于包含復(fù)雜大數(shù)據(jù)的納米等離子體光譜,從而降低納米等離子體生物傳感的有效性。
相比之下,人工智能 (AI) 可以從多個領(lǐng)域提取數(shù)據(jù)特征,從而增強納米等離子體光譜的模式識別能力,并提高納米等離子體生物傳感的效率。對于 sEV 光譜分析,由于納米等離子體響應(yīng)的高維性、連續(xù)性和物理相關(guān)性,有效捕捉細(xì)微的連續(xù)光譜偏移并解釋多維特征的貢獻(xiàn)仍然具有挑戰(zhàn)性。為了解決這個問題,該研究采用了柯爾莫戈洛夫-阿諾德網(wǎng)絡(luò) (KAN),它通過基于樣條函數(shù)的變換自適應(yīng)地學(xué)習(xí)優(yōu)化的激活函數(shù)。這種方法在建模光譜連續(xù)體方面具有卓越的能力,并且能夠明確解釋各個波長區(qū)域如何有助于預(yù)測,從而克服了傳統(tǒng) CNN 或Transformer 的主要局限性,這些傳統(tǒng) CNN 或 Transformer 在處理這種復(fù)雜的光譜數(shù)據(jù)時,往往會受到不靈活的歸納偏差或缺乏固有的可解釋性的影響。
該研究提出了一種基于 KAN 深度學(xué)習(xí)的納米等離子體生物傳感方法,用于高靈敏度檢測血清中的 sEV,從而促進(jìn) PDAC 篩查。該研究開發(fā)了一種晶圓級周期性納米等離子體金納米孔芯片,用于靶向高通量檢測臨床血清中的兩種 PDAC特異性 sEV 膜蛋白(GPC1 和 EphA2)。獲取的光譜信息進(jìn)一步使用 KAN 深度學(xué)習(xí)進(jìn)行全局分析。在此過程中,模型分析整個光譜以將每個信號分類為對照或 PDAC,特別突出了三個關(guān)鍵效應(yīng)的演變。在實驗中,研究隊列包括 600 名PDAC 患者和 1200 名對照,包括一個獨立的外部驗證集(120 名 PDAC/240名對照),用于評估這種傳感方式在 PDAC 中的診斷性能。對照組包括900例肝癌(HC)、100例胰腺炎患者、100例膽管癌(CCA)患者和100例肝細(xì)胞癌(HCC)患者。將模型輸出與傳統(tǒng)納米等離子體傳感方法下所有共振波長位置的單獨和組合分析結(jié)果進(jìn)行比較,結(jié)果顯示診斷結(jié)果更佳。值得注意的是,與傳統(tǒng)方法相比,基于KAN的納米等離子體生物傳感方法的曲線下面積(AUC)提高了58.9%。這些結(jié)果凸顯了KAN驅(qū)動的深度學(xué)習(xí)納米等離子體sEV平臺在PDAC檢測中增強的傳感性能。此外,該研究開發(fā)的方法可以擴展到其他癌癥篩查應(yīng)用中的腫瘤特異性sEV分析。
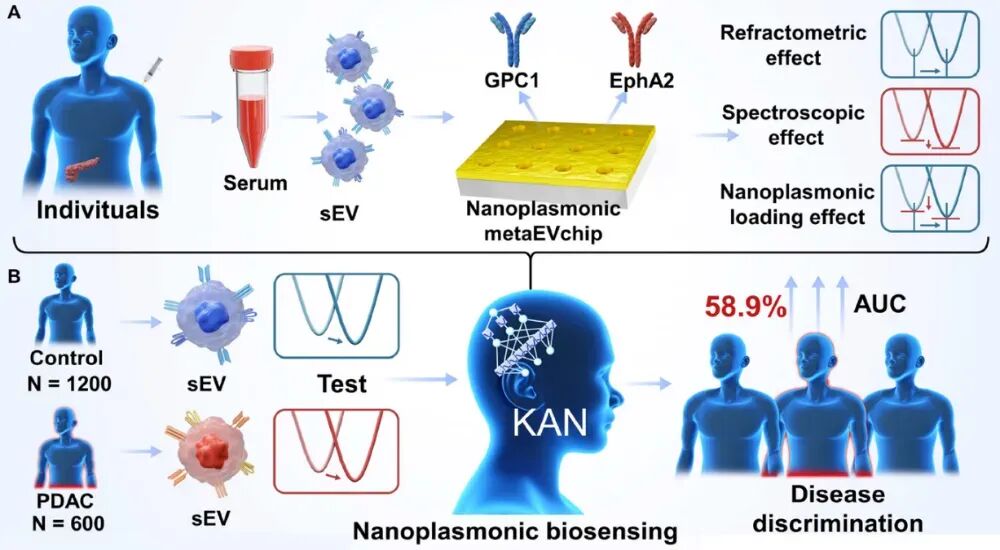
圖1 KAN驅(qū)動的納米等離子體生物傳感方法示意圖,用于sEV檢測以促進(jìn)PDAC篩查(圖源自Advanced Science) 參考消息:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202511337
來源:iNature
-
生物傳感
+關(guān)注
關(guān)注
0文章
61瀏覽量
11255
發(fā)布評論請先 登錄
中微愛芯與工信部電子第五研究所達(dá)成戰(zhàn)略合作
中國科大:提出基于拓?fù)?b class='flag-5'>超構(gòu)表面的可穿戴生物傳感技術(shù)

云知聲榮登2025胡潤中國人工智能企業(yè)50強榜單
深圳爭妍微電子獲2025年度全國鄉(xiāng)村振興先進(jìn)單位殊榮

湃睿科技受邀參加第8屆中國精準(zhǔn)醫(yī)療大會共探“AI+精準(zhǔn)醫(yī)療”創(chuàng)新發(fā)展

翼輝信息亮相2025長春航空展
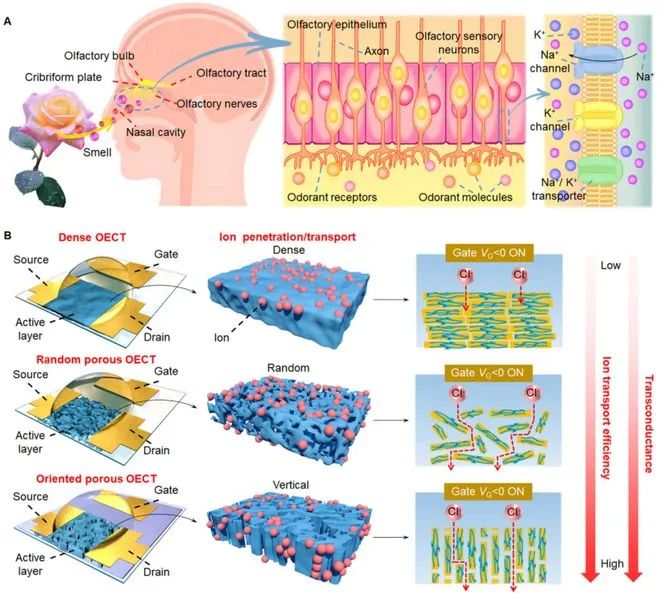
同濟(jì)大學(xué):仿生納米通道氣凝膠晶體管,突破生物傳感靈敏度極限
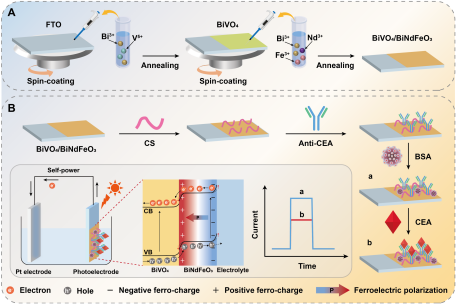
暨南大學(xué):鐵電極化調(diào)控的自供電、高靈敏PEC型腫瘤標(biāo)志物傳感技術(shù)
Gartner 發(fā)布2025年中國人工智能十大趨勢

上海交通大學(xué):研究面向呼吸監(jiān)測的超靈敏共價有機框架薄膜電阻式濕度傳感器納微快報




 中國人民解放軍總醫(yī)院第五醫(yī)學(xué)中心:研究開發(fā)的metaEVchip生物傳感策略可用于血清中超靈敏的sEV分析
中國人民解放軍總醫(yī)院第五醫(yī)學(xué)中心:研究開發(fā)的metaEVchip生物傳感策略可用于血清中超靈敏的sEV分析




評論