經顱聚焦超聲刺激(tFUS)參數效應概述
經顱聚焦超聲刺激(tFUS)作為一種非侵入性神經調節技術,其核心優勢在于通過精確調控超聲參數實現對神經活動的雙向調節(興奮或抑制)。參數選擇直接決定聲波在顱內的傳播效率、空間靶向性及生理效應。研究表明,tFUS的神經調制效果并非由單一參數主導,而是多參數協同作用的結果。例如,高頻脈沖重復頻率(PRF)和高占空比(DC)傾向于激發興奮性響應,而低強度、長時程刺激則易誘導抑制性效應。這種參數-效應關系源于超聲對神經元膜電位、離子通道和突觸可塑性的機械生物學影響,為精準治療神經系統疾病提供了理論基礎。

圖1: 核心參數與神經調制效應示意圖
圖1通過可視化元素概括了tFUS的核心參數(頻率f0、強度Ispta/Isppa、聲波持續時間SD、脈沖重復頻率PRF、占空比DC)及其與神經調制效應(興奮性 vs. 抑制性)的關聯。
關鍵信息:
興奮性調制采用“高強度、高PRF、高DC、短SD”組合,旨在快速激活神經元。
抑制性調制采用“低強度、低PRF、低DC、長SD”組合,傾向于持久抑制神經活動。
科學意義:該圖提供了參數-效應的直觀框架,揭示了多參數協同而非孤立作用的核心原則。例如,高PRF和高DC通過增強能量累積促進興奮,而低參數組合通過溫和持續刺激激活抑制通路。這種二分法為后續表格中的實驗協議奠定了理論基礎,突出了tFUS的可編程性。
HUIYING
核心參數及其神經調節效應概述
以下對tFUS的五個關鍵參數進行分述,每個參數均基于文獻證據說明其作用機制和效應趨勢:
超聲頻率(f0):頻率是平衡穿透深度與空間分辨率的關鍵參數。低頻(如200-650 kHz)對應較長波長,能有效穿透顱骨并減少衰減,適用于深部腦區靶向(如丘腦或基底節),但空間分辨率較低(焦點直徑約2-4 mm)。高頻(>1 MHz)可實現毫米級精準聚焦,但能量衰減顯著,限制其臨床應用。頻率本身不直接決定興奮或抑制,而是優化聲波傳輸效率,為其他參數調制提供基礎。例如,研究顯示f0低于700 kHz時,顱骨傳輸效率最高,確保能量足量到達目標腦區。
占空比(DC):DC定義脈沖有效時間占周期的比例,直接影響熱效應和神經元選擇性激活。低DC(<5%)通過激活T型鈣通道偏好抑制性神經元(如 thalamic reticular neurons),產生網絡抑制;高DC(>20%)則興奮興奮性神經元(如錐體細胞)。動物實驗表明,70% DC刺激運動皮層可最大化興奮響應,而5% DC誘導抑制。DC需謹慎控制以避免熱損傷,通常采用脈沖式而非連續波以最小化熱積累。
脈沖重復頻率(PRF):PRF決定脈沖發放密度,與神經元的頻率響應特性相關。高PRF(>100 Hz,如500-3000 Hz)增強興奮性神經元放電,呈劑量依賴性增加運動誘發電位(MEP)振幅;低PRF(5-100 Hz)抑制神經活動,如10 Hz PRF降低MEP振幅達60分鐘。機制上,興奮性神經元對高PRF敏感,而抑制性神經元響應較弱,這種差異性使PRF成為調節興奮-抑制平衡的重要杠桿。
聲波持續時間(SD):SD決定總能量輸入,短SD(<500 ms)易引發瞬時興奮(如誘發動作電位),長SD(≥1 s)導致持續抑制。例如,毫秒級SD激活運動皮層產生肢體運動,而9秒SD抑制視覺誘發電位。SD與能量累積相關,短時刺激避免適應性代償,長時刺激可能激活抑制性可塑性通路。
超聲強度(I):強度參數包括空間峰值時間平均強度(Ispta,關聯熱風險)和空間峰值脈沖強度(Isppa,反映機械力)。低Isppa(0.1-1 W/cm2)激活高敏感性抑制神經元(如LTS細胞),高Isppa(>1 W/cm2)興奮低敏感性神經元(如RS細胞)。強度需平衡效應與安全,過高Ispta(>3.7 W/cm2)可能逆轉為抑制或因熱效應致傷,FDA建議Ispta<94 mW/cm2以控制風險。

圖2:超聲神經調控刺激參數定義與關系示意圖
圖2通過示意圖形式系統性地展示了 transcranial focused ultrasound(tFUS) 神經調控中聲波的基本參數及其數學關系,這些參數是理解超聲刺激生物效應和優化刺激協議的核心。該圖首先定義了聲波的兩個基本物理量:強度(表示波幅大小)和瞬時周期(T),后者用于計算聲學頻率(Af),即單位時間內的振蕩周期數(對應方程1)。此外,刺激持續時間(SD)表示單次超聲作用的總體時長,而刺激模式分為連續式或脈沖式;針對脈沖范式,圖2進一步引入了脈沖持續時間(PD,即單次聲波振蕩的時長)和脈沖重復周期(PRP,即連續兩次脈沖起始點之間的間隔),后者用于計算脈沖重復頻率(PRF)(對應方程2)。
圖2中還明確了占空比(DC)的概念,即脈沖持續時間占脈沖重復周期的比例(方程3),以及每個脈沖內的周期數(c/p)和刺激期間的總脈沖數(Np)(分別對應方程4和方程5)。這些參數共同構成了 tFUS 刺激協議的基礎,通過調控它們(如增加PD或調整PRF),可以精確調節聲波的能量沉積和時空特性,從而影響神經膜的機械應力(如激活電壓門控離子通道或誘導膜孔隙形成),最終實現抑制或促進神經活動的效果。
HUIYING
參數組合如何實現不同效應
tFUS的神經調節效應依賴參數間的協同作用,而非孤立變化。興奮性與抑制性協議通過系統化組合實現差異化輸出:
興奮性組合:采用“高強度、高PRF、高DC、短SD”。例如,表1中的人類研究使用500 Hz PRF、50% DC和300 ms SD刺激體感皮層,增強誘發電位;動物模型中,1000 Hz PRF與50% DC結合促進卒中后運動功能恢復。這種組合通過高能量輸入和密集脈沖同步激活興奮性環路,并抑制抑制性中間神經元。
抑制性組合:基于“低強度、低PRF、低DC、長SD”。如表2所示,10 Hz PRF、5% DC和120 s SD刺激運動皮層,降低MEP振幅并增強GABA能抑制;在癲癇模型中,低參數組合減少發作頻率。此類方案通過溫和持續刺激激活抑制性微電路,促進長時程抑制(LTD)樣可塑性。
參數組合的效應可通過神經細胞內空化興奮(NICE)模型解釋:不同參數配置偏好特定神經元亞群,如低DC/低PRF靶向抑制性鈣通道,而高DC/高PRF驅動興奮性鈉通道。
HUIYING
"在線效應"與"離線效應"與tFUS參數關聯概述
在線效應:指刺激期間的即時神經響應,由超聲機械力直接調控膜電位和離子通道(如機械敏感通道TRAAK)。參數如短SD(<100 ms)和高Isppa可瞬時去極化神經元,誘發動作電位;低PRF則實時抑制放電。在線效應依賴參數瞬時值,效應隨刺激停止而消失。
離線效應:指刺激后持續數分鐘至小時的可塑性變化,涉及分子級聯反應,如Ca2?信號觸發激酶活化、基因表達調控(如c-Fos上調)和突觸重塑。離線效應與參數時序結構相關:高頻節律封裝(如theta爆發式PRF)誘導LTP樣興奮性可塑性,而低PRF長時程刺激累積抑制性信號。參數策略上,離線效應需滿足“能量閾值+時序共振”,例如高PRF(2000 Hz)結合適中DC(40%)可延長MEP增強至30分鐘,而低DC(5%)長SD(30 s)產生持續鎮痛。
關聯性上,參數決定效應從機械門控向分子可塑性的過渡:在線效應由SD、PRF等瞬時參數主導,離線效應則依賴DC、強度等可持續驅動可塑性通路的參數。
HUIYING
參數如何控制安全性
安全性由參數嚴格約束,以規避機械和熱損傷:
機械指數(MI)控制:MI(與聲壓相關)需<1.9,防止空化效應。爭議案例中MI超閾值(3.4-4.0)導致腦損傷,強調實測顱內聲壓的必要性。
熱效應管理:低頻率(200-650 kHz)和脈沖式刺激減少顱骨吸熱;短SD和低PRF限制能量累積。合規參數下(如Ispta<94 mW/cm2),組織溫升<1.5°C,無病理損傷。
標準化與監測:遵循ITRUSST指南,全面報告驅動系統和顱內暴露水平。動物和臨床研究(共677例)顯示,合規參數下不良反應率僅3.4%(如短暫頭痛),無永久性損傷,驗證tFUS在優化參數下的高安全性。
HUIYING
總結
tFUS通過多參數精細調控實現神經環路的精準調制,參數-效應關系已成為其臨床轉化的核心。未來需構建標準化參數體系,結合多模態監控(如EEG頻帶分析)量化調節效果,并通過大樣本試驗驗證其在腦疾病治療中的潛力。參數化策略不僅提升療效可重復性,也為個體化神經調節開辟了新途徑。
-
超聲
+關注
關注
1文章
120瀏覽量
22214 -
醫療電子
+關注
關注
31文章
1454瀏覽量
92209
發布評論請先 登錄
PID調參的相關資料分享
針對PID調參進行詳細的講解
告別調參煉丹,使用隨機共享權重足矣!

什么是調參 CCP協議的實現原理
NNI:自動幫你做機器學習調參的神器
PID參數整定實際調參
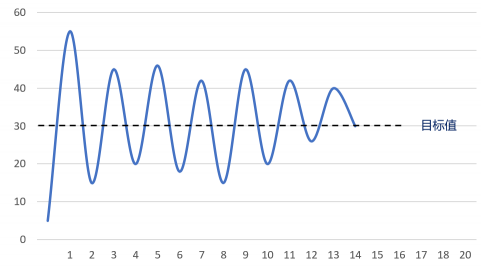
機器學習8大調參技巧

LSTM神經網絡的調參技巧
BP神經網絡的調參技巧與建議
tFUS+HD-tDCS如何實現毫米級皮層精準調控?




 tFUS如何精準調參實現神經活動的雙向調節?
tFUS如何精準調參實現神經活動的雙向調節?




評論