在藥品生產(chǎn)與質(zhì)量管理的數(shù)字化進(jìn)程中,電子時(shí)間戳已成為證明數(shù)據(jù)完整性的核心要素。對(duì)于面向國際市場的制藥企業(yè)而言,理解FDA對(duì)電子時(shí)間戳的最新要求,不僅是滿足監(jiān)管合規(guī)的底線,更是構(gòu)建可信數(shù)據(jù)體系的基礎(chǔ)。2024年10月,F(xiàn)DA發(fā)布了關(guān)于臨床研究中電子系統(tǒng)、電子記錄和電子簽名的最新指南,這是自2003年以來該領(lǐng)域首次重大更新。這一動(dòng)向釋放出明確信號(hào):時(shí)間戳的管理正從“技術(shù)細(xì)節(jié)”上升為“合規(guī)焦點(diǎn)”。
第一部分:FDA對(duì)電子時(shí)間戳的核心要求解析
FDA對(duì)電子時(shí)間戳的要求,根植于21 CFR Part 11法規(guī)及其配套指南。這套規(guī)范的核心,是為電子記錄建立與紙質(zhì)記錄同等的可信度。
時(shí)間戳必須納入強(qiáng)制性的審計(jì)追蹤體系。 根據(jù)21 CFR Part 11 §11.10(a)的規(guī)定,系統(tǒng)必須具備“計(jì)算機(jī)生成的、帶時(shí)間戳的審計(jì)追蹤功能”,以記錄操作者身份、操作時(shí)間和操作內(nèi)容。這意味著,任何電子記錄的創(chuàng)建、修改、刪除或簽署行為,都必須自動(dòng)生成包含精確時(shí)間戳的記錄,且該功能不能被用戶關(guān)閉,記錄一旦生成即不可篡改。對(duì)于藥廠的時(shí)鐘系統(tǒng)而言,這要求其輸出的時(shí)間戳必須能夠無縫集成到LIMS、MES等核心系統(tǒng)的審計(jì)追蹤中,形成完整的證據(jù)鏈。
時(shí)間同步性是ALCOA+原則的核心要素。 FDA強(qiáng)調(diào)電子記錄必須遵循ALCOA+原則,其中“同步性(Contemporaneous)”要求數(shù)據(jù)在產(chǎn)生時(shí)即被記錄,而非事后補(bǔ)錄。這一原則的實(shí)現(xiàn),依賴于所有數(shù)據(jù)采集點(diǎn)(從生產(chǎn)設(shè)備到檢驗(yàn)儀器)的時(shí)間基準(zhǔn)完全統(tǒng)一。如果不同設(shè)備的時(shí)間存在偏差,即使每個(gè)設(shè)備都生成了時(shí)間戳,也無法滿足“同步記錄”的合規(guī)要求。
時(shí)間戳的完整性與可追溯性貫穿記錄全生命周期。 根據(jù)FDA指南,電子記錄在整個(gè)保存期內(nèi)必須受到保護(hù),防止未經(jīng)授權(quán)的訪問和篡改。這意味著時(shí)間戳不能孤立存在,而必須與記錄內(nèi)容、操作者身份、簽名含義等元數(shù)據(jù)綁定,形成不可分割的數(shù)字封包。同時(shí),審計(jì)追蹤記錄的保存期限必須與主體記錄一致——制藥行業(yè)通常要求10年以上。
 時(shí)鐘照片
時(shí)鐘照片
第二部分:藥廠如何構(gòu)建符合FDA要求的時(shí)間管理體系
面對(duì)FDA對(duì)電子時(shí)間戳的嚴(yán)苛要求,藥廠需要從系統(tǒng)架構(gòu)、設(shè)備選型和流程管理三個(gè)層面構(gòu)建合規(guī)的時(shí)間管理體系。
建立權(quán)威、可溯源的統(tǒng)一時(shí)間基準(zhǔn)是根本前提。 系統(tǒng)必須采用可信的時(shí)間源,如北斗/GPS雙模衛(wèi)星授時(shí),確保時(shí)間戳可追溯至國家標(biāo)準(zhǔn)時(shí)間。同時(shí),應(yīng)配置主備冗余的時(shí)間服務(wù)器,確保單點(diǎn)故障時(shí)時(shí)間服務(wù)不中斷。對(duì)于多廠區(qū)企業(yè),需建立分層同步架構(gòu),確保所有生產(chǎn)、檢驗(yàn)、倉儲(chǔ)區(qū)域的時(shí)間基準(zhǔn)完全一致。
系統(tǒng)驗(yàn)證與審計(jì)追蹤是合規(guī)的核心保障。 FDA要求系統(tǒng)必須經(jīng)過充分驗(yàn)證,以證明其“適合預(yù)期用途且能持續(xù)一致地運(yùn)行”。這包括安裝確認(rèn)(IQ)、運(yùn)行確認(rèn)(OQ)和性能確認(rèn)(PQ)的完整文檔包。時(shí)鐘系統(tǒng)作為時(shí)間基準(zhǔn)源,其驗(yàn)證記錄必須納入藥廠的質(zhì)量管理體系。同時(shí),時(shí)間服務(wù)器必須生成不可篡改的運(yùn)行日志,記錄所有同步狀態(tài)、配置變更和異常事件,并支持按需導(dǎo)出供審計(jì)審查。
遠(yuǎn)程監(jiān)控與主動(dòng)預(yù)警能力提升合規(guī)管理水平。 具備集中管理功能的時(shí)鐘系統(tǒng),可以實(shí)時(shí)監(jiān)控全廠所有時(shí)鐘的同步狀態(tài),當(dāng)檢測到時(shí)間偏差超限或同步失敗時(shí)自動(dòng)告警。這種主動(dòng)維護(hù)能力,能夠?qū)撛诘臅r(shí)間偏移風(fēng)險(xiǎn)消滅在萌芽狀態(tài),避免因時(shí)間不準(zhǔn)導(dǎo)致的批次數(shù)據(jù)完整性問題。
 時(shí)鐘照片
時(shí)鐘照片
因此,F(xiàn)DA對(duì)電子時(shí)間戳的最新要求,實(shí)質(zhì)上是將“時(shí)間”這一基礎(chǔ)要素納入了數(shù)據(jù)完整性的核心管理體系。對(duì)于藥廠而言,選擇一套具備權(quán)威時(shí)間源、完整審計(jì)追蹤、系統(tǒng)驗(yàn)證支持和遠(yuǎn)程監(jiān)控能力的時(shí)間同步方案,不僅是應(yīng)對(duì)監(jiān)管審計(jì)的務(wù)實(shí)之選,更是為每一份藥品數(shù)據(jù)鑄造可信“時(shí)間印記”的戰(zhàn)略投資。
以上就是“FDA對(duì)電子時(shí)間戳的最新指南是什么?”的全部內(nèi)容了,述泰時(shí)鐘15年專注為醫(yī)療業(yè),教育業(yè),交通業(yè),公安,政府機(jī)關(guān)等領(lǐng)域研發(fā)生產(chǎn)同步時(shí)鐘,電子萬年歷,時(shí)間服務(wù)器,支持北斗GPS衛(wèi)星同步,4G無線,NTP網(wǎng)絡(luò),Wifi等校時(shí)方式,為客戶提供好用的電子鐘秒同步產(chǎn)品和時(shí)間同步方案,讓企業(yè)實(shí)現(xiàn)時(shí)間精準(zhǔn)同步,實(shí)現(xiàn)組織高效率,高協(xié)同,高標(biāo)準(zhǔn)的辦公環(huán)境,是中國胸痛中心大會(huì)多年的贊助商。
審核編輯 黃宇
-
時(shí)鐘
+關(guān)注
關(guān)注
11文章
1998瀏覽量
135196 -
FDA
+關(guān)注
關(guān)注
0文章
84瀏覽量
19164
發(fā)布評(píng)論請(qǐng)先 登錄
電網(wǎng)并網(wǎng)新規(guī)下,分布式光伏企業(yè)如何合規(guī)運(yùn)行?

求助,關(guān)于TJA1103硬件時(shí)間戳問題求解
深度剖析LTC4263:IEEE 802.3af合規(guī)PSE控制器的卓越之選
燈具EMC測試全解析|合規(guī)入市核心指南

醫(yī)療器械 FDA 認(rèn)證 (510k/PMA) 解析與研發(fā)管線合規(guī)實(shí)踐 (附 ALM 工具鏈方案)

開發(fā)智能體配置-內(nèi)容合規(guī)
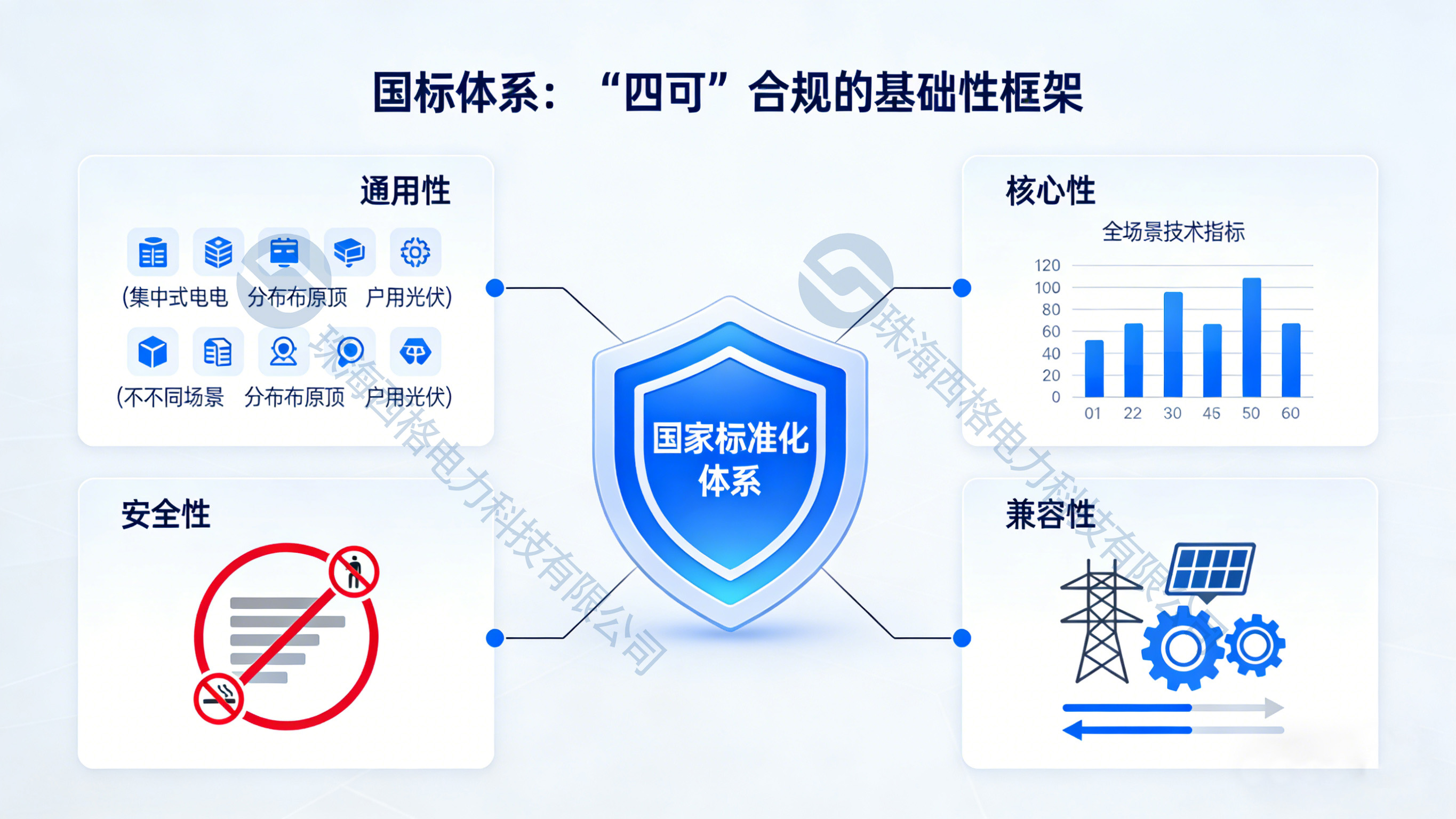
“四可”標(biāo)準(zhǔn)體系解析:國標(biāo)與電網(wǎng)接入規(guī)范的合規(guī)性指南
中美芯片政策調(diào)整,瑞之辰以合規(guī)創(chuàng)新錨定增長

百億罰單警示下的破局之道:DXC數(shù)據(jù)合規(guī)實(shí)踐案例

RFID技術(shù)對(duì)冷鏈物流溫控合規(guī)性的價(jià)值貢獻(xiàn)
是德科技推出HDMI 2.2物理層合規(guī)性測試解決方案

汽車軟件團(tuán)隊(duì)必看:基于靜態(tài)代碼分析工具Perforce QAC的ISO 26262合規(guī)實(shí)踐

解鎖制藥新質(zhì)生產(chǎn)力:合規(guī)與效率雙贏的數(shù)字化轉(zhuǎn)型之道
汽車電子開發(fā)必備:基于Perforce ALM的ISO 26262合規(guī)認(rèn)證指南




 合規(guī)之錨:FDA對(duì)電子時(shí)間戳的最新指南與藥廠應(yīng)對(duì)之道
合規(guī)之錨:FDA對(duì)電子時(shí)間戳的最新指南與藥廠應(yīng)對(duì)之道





評(píng)論