引言:在前面我們了解了如何使用TCGAbiolinks檢索并獲取TCGA數據庫的公開數據。今天小編就用前面涉及到的代碼,下載今天數據準備需要用到的TCGA樣本數據。
一、數據下載階段
第一步:GDCquery()篩選我們需要的數據,TCGAbiolinks包下載TCGA數據進行表達差異分析-肝癌案例
library("TCGAbiolinks")
query <- GDCquery(project = "TCGA-LIHC",
data.category = "Transcriptome Profiling",
data.type = "Gene Expression Quantification",
workflow.type = "HTSeq - Counts")
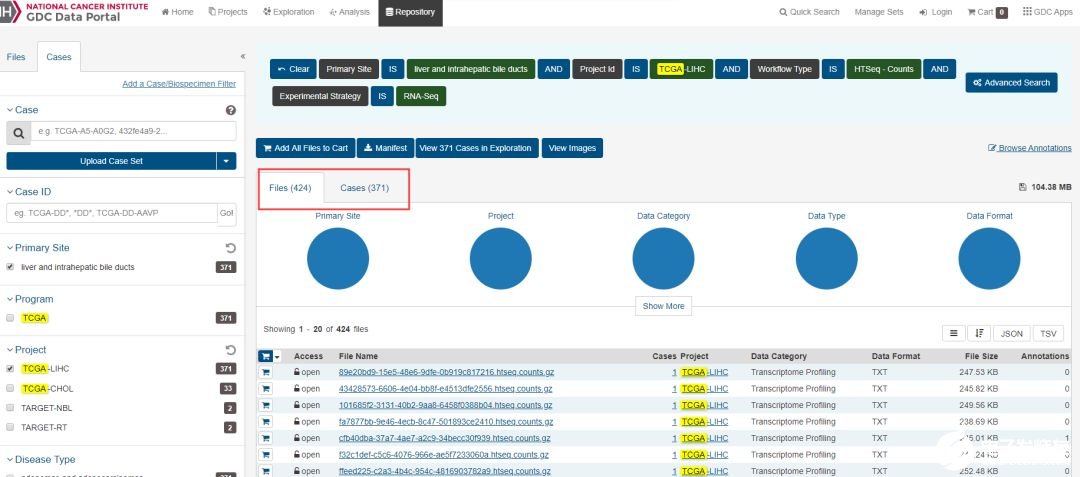
上圖為通過TCGA GDC鏈接中根據篩選條件查看的符合要求結果。下圖為通過GDCquery()函數中傳入對應的參數得到的結果。兩者對比,我們可以發現,兩者是一模一樣的。說明代碼執行正確。前面一期中,我們有詳細談及 GDCquery,可做參考。
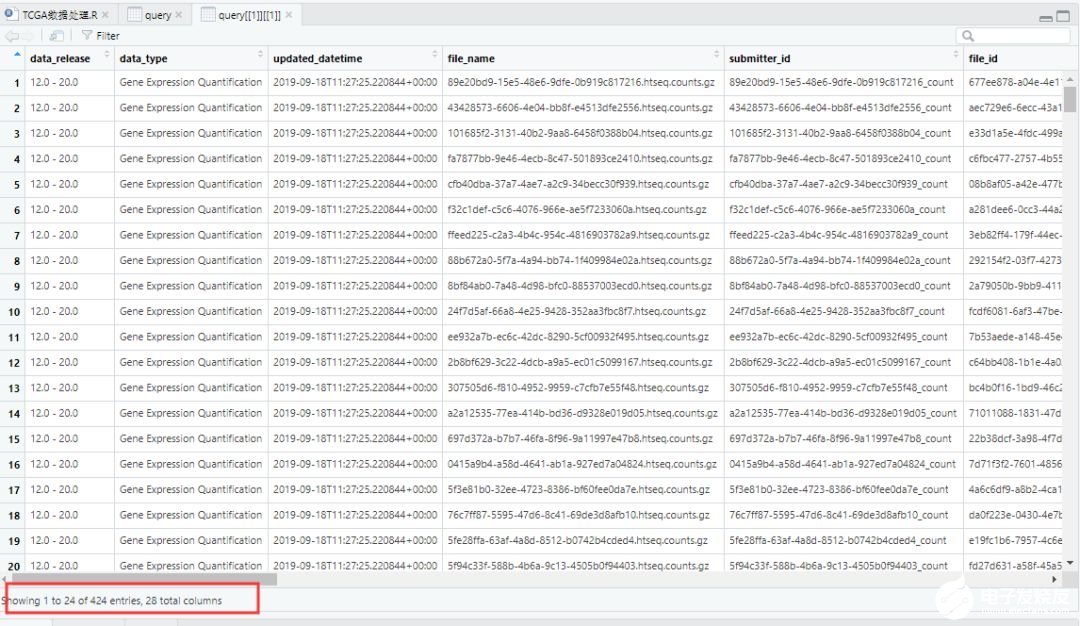
samplesDown <- getResults(query,cols=c("cases"))
#getResults(query, rows, cols)根據指定行名或列名從query中獲取結果,此處用來獲得樣本的barcode
# 此處共檢索出424個barcodes
getResults()中用到的參數:
參數用法query
來自GDCquery的結果rows用于指定特定的行cols用于指定特定的列
# 從samplesDown中篩選出TP(實體腫瘤)樣本的barcodes
# TCGAquery_SampleTypes(barcode, typesample)
# TP代表PRIMARY SOLID TUMOR;NT-代表Solid Tissue Normal(其他組織樣本可參考學習文檔)
##此處共檢索出371個TP樣本barcodes
dataSmTP <- TCGAquery_SampleTypes(barcode = samplesDown,
typesample = "TP")
# 從samplesDown中篩選出NT(正常組織)樣本的barcode
#此處共檢索出50個NT樣本barcodes
dataSmNT <- TCGAquery_SampleTypes(barcode = samplesDown,
typesample = "NT")
TCGAquery_SampleTypes中的參數詳解:
參數用法barcodeTCGA中的barcodes列表typesample用于指定篩選哪種類型的組織樣本,如腫瘤組織“TP”,正常組織“NT”
補充TCGA中的組織樣本類型:
TPPRIMARY SOLID TUMORTMMetastaticTRRECURRENT SOLID TUMORTAMAdditional MetastaticTBPrimary Blood Derived Cancer-Peripheral BloodTHOCHuman Tumor Original CellsTRBMRecurrent Blood Derived Cancer-Bone MarrowTBM Primary Blood Derived Cancer-Bone MarrowTAPAdditional-New PrimaryNB Blood Derived Normal NTSolid Tissue NormalNBCBuccal Cell Normal???NEBVEBV Immortalized NormalNBMBone Marrow Normal
###設置barcodes參數,篩選符合要求的371個腫瘤樣本數據和50正常組織數據
queryDown <- GDCquery(project = "TCGA-LIHC",
data.category = "Transcriptome Profiling",
data.type = "Gene Expression Quantification",
workflow.type = "HTSeq - Counts",
barcode = c(dataSmTP, dataSmNT))
#barcode參數:根據傳入barcodes進行數據過濾
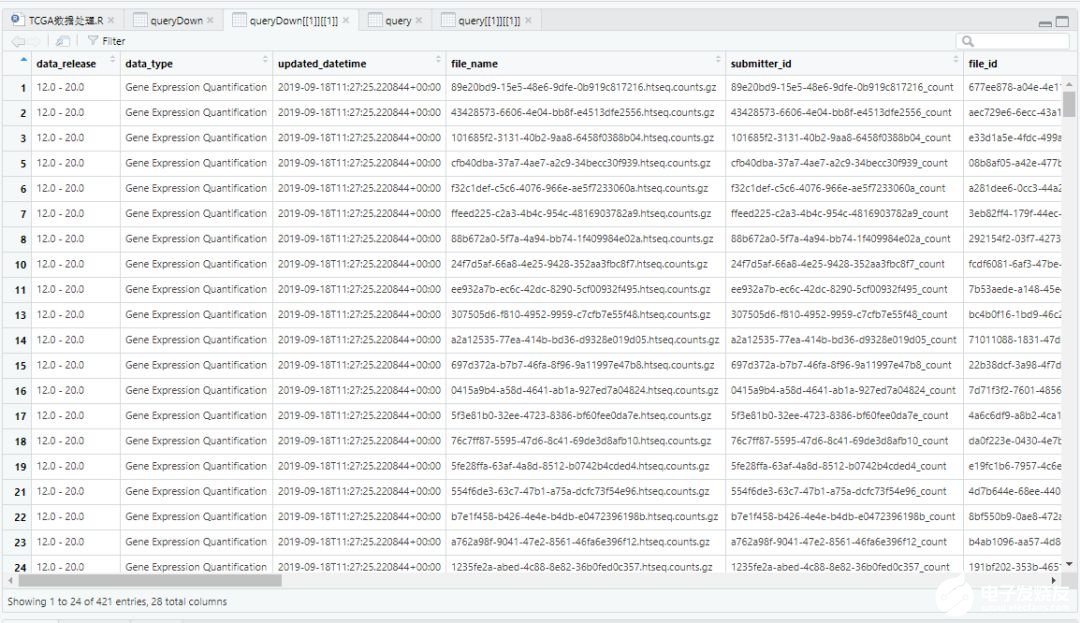
上圖為 queryDown<-GDCquery()的結果,僅選擇了選擇371個正常組織和50個腫瘤組織樣本。
第二步:GDCdownload()下載GDCquery()得到的結果
# 下載數據,默認存放位置為當前工作目錄下的GDCdata文件夾中。
GDCdownload(queryDown,method = "api", directory = "GDCdata",
files.per.chunk = 10)
#method ;"API"或者"client"。"API"速度更快,但是容易下載中斷。
#directory:下載文件的保存地址。Default: GDCdata。
#files.per.chunk = NULL:使用API下載大文件的時候,可以把文件分成幾個小文件來下載,可以解決下載容易中斷的問題。
GDCdownload(query = queryDown)

說明:由于小編前面已經下載過該TCGA數據,所以這里顯示的是421個文件已存在。如果還沒有下載的話,可能需要根據自己的網速等待一些時間。
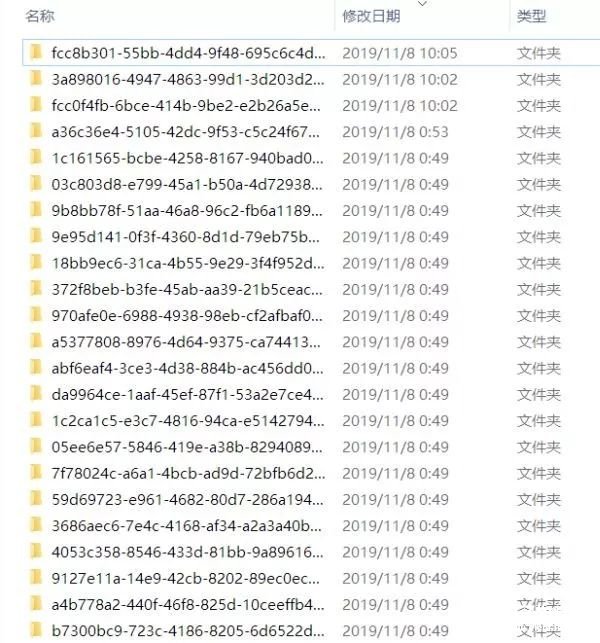
顯示這樣的結果,就算下載成功啦!文件默認保存在 Rstudio默認路徑下的GDCdata中。前面就是我們利用第一期知識進行數據下載環節,權當溫習功課吧——接下來我們就開始此期的數據處理~~
二、數據處理
第三步:GDCprepare()將前面GDCquery()的結果準備成R語言可處理的SE(SummarizedExperiment)文件。
#讀取下載的數據并將其準備到R對象中,在工作目錄生成(save=TRUE)LIHC_case.rda文件
# GDCprepare():Prepare GDC data,準備GDC數據,使其可用于R語言中進行分析
dataPrep1 <- GDCprepare(query = queryDown, save = TRUE, save.filename =
"LIHC_case.rda")
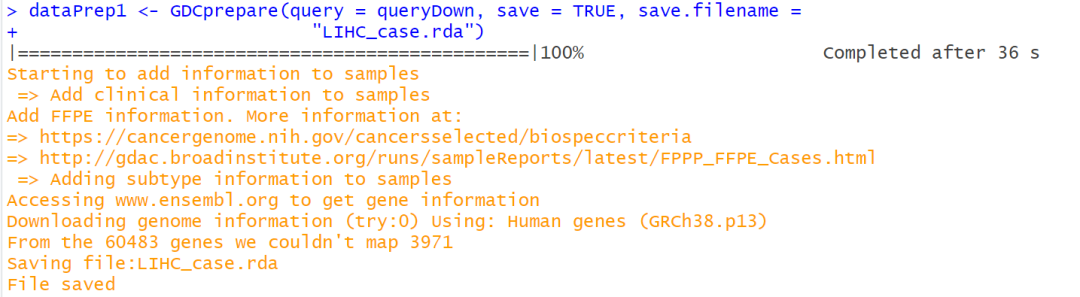
GDCprepare()中的參數:
參數用法query來自GDCquery的結果save是否將結果保存為RData object,默認為TRUEsave.filename文件名,如果沒有設置,系統將默認設置directory文件數據的文件夾,默認為“GDCdata”summarizedExperiment是否生成summarizedExperiment對象,默認TRUE
第四步:TCGAanalyze_Preprocessing()對數據進行預處理:使用spearman相關系數去除數據中的異常值
# 去除dataPrep1中的異常值,dataPrep1數據中含有腫瘤組織和正常組織的數據
# TCGAanalyze_Preprocessing(object, cor.cut = 0, filename = NULL,
width = 1000, height = 1000, datatype = names(assays(object))[1])
# 函數功能描述:Array Array Intensity correlation (AAIC) and correlation boxplot to define outlier
dataPrep2 <- TCGAanalyze_Preprocessing(object = dataPrep1,
cor.cut = 0.6,
datatype = "HTSeq - Counts")
#將預處理后的數據dataPrep2,寫入新文件“LIHC_dataPrep.csv”
write.csv(dataPrep2,file = "LIHC_dataPrep.csv",quote = FALSE)
這里將生成一個array-array intensity correlation(AAIC)相關性熱圖,如下:
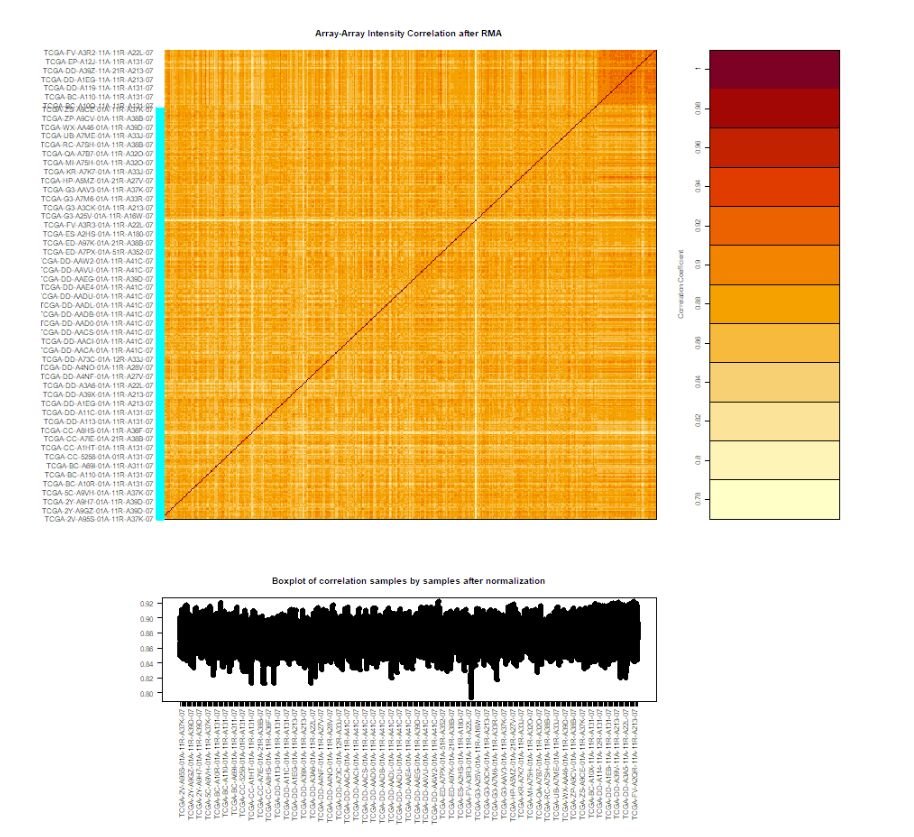
TCGAanalyze_Preprocessing()中的參數:
參數用法object來自TCGAprepare的結果cor.cut設置閾值,根據樣本中各個樣本之間的spearman相關系數進行過濾。默認為0filename設置生成圖片文件的名稱,默認為PreprocessingOutput.pngwidth生成圖片的寬度?? height生成圖片的高度datatype描述RangedSummarizedExperiment 數據類型的字符串
第五步:TCGAtumor_purity()篩選腫瘤純度大于60%的腫瘤barcodes
# TCGAtumor_purity(barcodes, estimate, absolute, lump, ihc, cpe),使用來自5種方法的5個估計值作為閾值對TCGA樣本進行過濾,這5個值是estimate, absolute, lump, ihc, cpe,這里設置cpe=0.6(cpe是派生的共識度量,是將所有方法的標準含量歸一化后的均值純度水平,以使它們具有相等的均值和標準差)
#篩選腫瘤純度大于等于60%的樣本數據
purityDATA <- TCGAtumor_purity(colnames(dataPrep1), 0, 0, 0, 0, 0.6)
# filtered 為被過濾的數據, pure_barcodes是我們要的腫瘤數據
Purity.LIHC<-purityDATA$pure_barcodes
normal.LIHC<-purityDATA$filtered
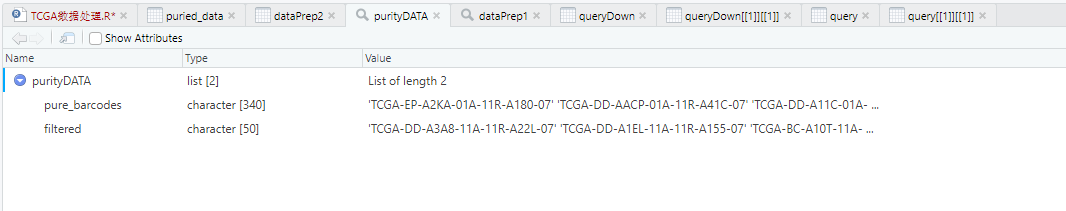
filtered 為被過濾的數據(為正常組織的數據barcodes), pure_barcodes是我們要的腫瘤樣本barcodes。
第六步:將腫瘤表達矩陣與正常組織表達矩陣合并,進行基因注釋
#獲取腫瘤純度大于60%的340個腫瘤組織樣本+50個正常組織樣本,共計390個樣本
puried_data <-dataPrep2[,c(Purity.LIHC,normal.LIHC)]
第七步:進行表達矩陣基因注釋
#基因注釋,需要加載“SummarizedExperiment”包,“SummarizedExperiment container”每個由數字或其他模式的類似矩陣的對象表示。行通常表示感興趣的基因組范圍和列代表樣品。
#if (!requireNamespace("BiocManager", quietly = TRUE))
install.packages("BiocManager")
#BiocManager::install("SummarizedExperiment") #沒有的需要執行下載代碼
library("SummarizedExperiment")
rowData(dataPrep1) #傳入數據dataPrep1必須為SummarizedExperiment對象
# DataFrame with 56512 rows and 3 columns
# ensembl_gene_id external_gene_name original_ensembl_gene_id
# <character> <character> <character>
# ENSG00000000003 ENSG00000000003 TSPAN6 ENSG00000000003.13
# ENSG00000000005 ENSG00000000005 TNMD ENSG00000000005.5
# ENSG00000000419 ENSG00000000419 DPM1 ENSG00000000419.11
# ENSG00000000457 ENSG00000000457 SCYL3 ENSG00000000457.12
#將結果寫入文件“puried.LIHC.cancer.csv”
rownames(puried_data)<-rowData(dataPrep1)$external_gene_name
write.csv(puried_data,file = "puried.LIHC.csv",quote = FALSE)
第八步:進行表達矩陣標準化和過濾,得到用于差異分析的表達矩陣
`TCGAanalyze_Normalization()`使用EDASeq軟件包標準化mRNA轉錄本和miRNA。
#TCGAanalyze_Normalization()執行EDASeq包中的如下功能:
1. EDASeq::newSeqExpressionSet
2. EDASeq::withinLaneNormalization
3. EDASeq::betweenLaneNormalization
4. EDASeq::counts
dataNorm <- TCGAanalyze_Normalization(tabDF = puried_data,
geneInfo = geneInfo,
method = "gcContent")
TCGAanalyze_Normalization中的參數:
參數用法tabDFRNAseq表達矩陣,行代表基因,列代表樣本geneInfo關于geneLength和gcContent的20531個基因的矩陣,“geneInfoHT”和“geneInfo”可選。method選擇標準化的方法,基于’gcContent’ 或 ’geneLength’的標準化方法可選
#將標準化后的數據再過濾,去除掉表達量較低(count較低)的基因,得到最終的數據
dataFilt <- TCGAanalyze_Filtering(tabDF = dataNorm,
method = "quantile",
qnt.cut = 0.25)
str(dataFilt)
#num [1:13083, 1:340] 274 2432 60347 1012 1947 ...
#- attr(*, "dimnames")=List of 2
# ..$ : chr [1:13083] "A1BG" "A1CF" "A2M" "A4GALT" ...
# ..$ : chr [1:390] "TCGA-DD-AAD5-01A-11R-A41C-07" "TCGA-DD-A4NO-01A-11R-A28V-07" "TCGA-EP-A2KA-01A-11R-A180-07" "TCGA-DD-AACP-01A-11R-A41C-07" ...
TCGAanalyze_Filtering()中的參數:
參數用法tabDF數據框或者矩陣,行代表基因,列代表來自TCGA的樣本method用于過濾較低count數的基因的方法,有’quantile’, ’varFilter’, ’filter1’, ’filter2’qnt.cut選擇均值作為過濾的閾值
最后將過濾后的數據寫入文件“TCGA_LIHC_final.csv”,就得到我們用于后續差異分析的表達文件:
write.csv(dataFilt,file = "TCGA_LIHC_final.csv",quote = FALSE)
#保留的是390個樣本(前340腫瘤,后50正常組織)
今天的數據預處理就講到這里,接下來我們將分享:數據分析(差異表達分析、富集分析和聚類分析等)。如果你喜歡的話,就加入我們一起挖數據吧~~
-
數據
+關注
關注
8文章
7335瀏覽量
94771 -
基因
+關注
關注
0文章
95瀏覽量
17794 -
數據預處理
+關注
關注
1文章
20瀏覽量
3000
發布評論請先 登錄



 如何使用TCGAbiolinks進行數據預處理?
如何使用TCGAbiolinks進行數據預處理?






評論